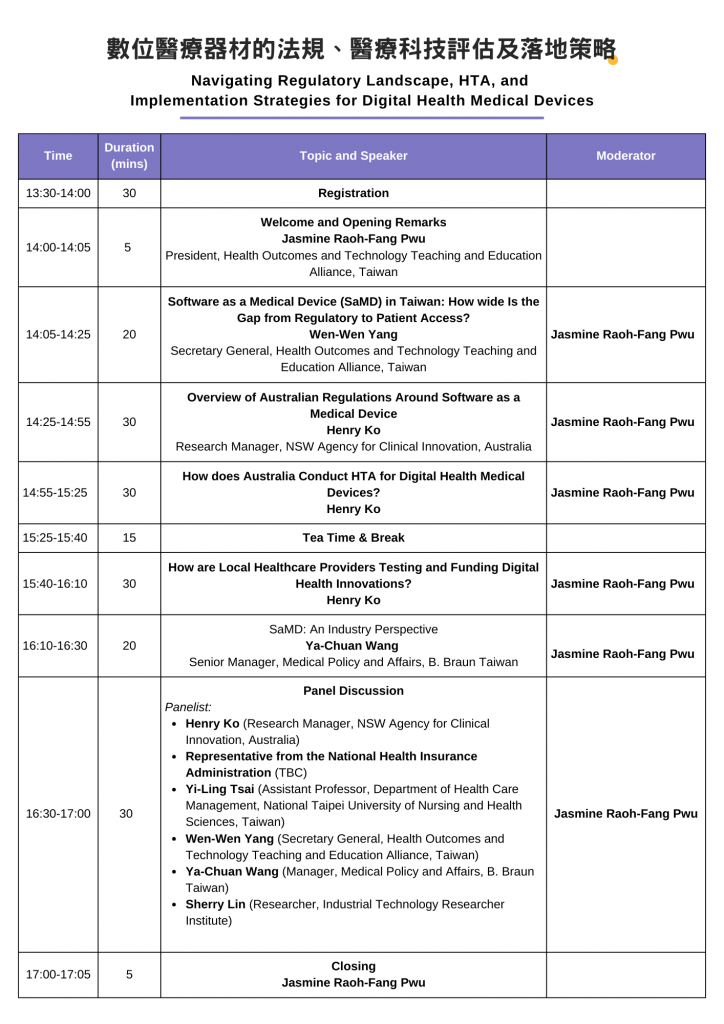
Navigating Regulatory Landscape, HTA, and Implementation Strategies for Digital Health Medical Devices
隨著數位技術不斷精進,近年來數位健康產品蓬勃發展,其中醫療器材軟體(software as a medical device, SaMD)更是發展迅速,迄今國內、外已有愈來愈多的SaMD完成開發並取得上市許可。為提升臺灣產業全球競爭力並加速產品邁入國內、外市場,2023年行政院生技產業策略諮議委員會(Bio Taiwan Committee, BTC)會議進一步指出納入健保為發展智慧醫療著手式之一,並建議協助國內研發製造或具外銷實力之創新醫療器材優先納入健保給付,並給予健保從優核價。對於如何協助已取得食品藥物管理署SaMD上市許可之產品進行HTA評估,以及如何決定產品於健保之價值項目,將是產學官界所需思考及共同面臨的議題。
為促成國內產學官界能透過國際經驗之分享及交流,本學會邀請有多年擔任澳洲植體收載委員會(Prostheses List Advisory Committee, PLAC)委員經驗的新南威爾斯臨床創新機構(NSW Agency for Clinical Innovation)研究經理 – Henry Ko博士,分享SaMD在澳洲從法規、HTA至收載的考量與經驗。此外安排我國SaMD的現況簡介及業界觀點,並邀請工業技術研究院及中央健康保險署長官交流及討論,期望帶給大家滿滿的收穫,共同促進SaMD產業良好的發展環境,以及提升病人照護品質。
活動日期及時間 Date and Time
2023年12月28日 星期四 13:30-17:05
13:30-17:05, Thursday, December 28, 2023
活動地點 Venue
張榮發國際會議中心
CHANG YUNG-FA FOUNDATION International Convention Center
地址 Address
台北市中正區中山南路11號8樓 801會議室
Room 801, 8F, No.11, Zhongshan S. Rd., Taipei City 10048, Taiwan (R.O.C.)
主辦單位 Host organization
健康效果暨醫療科技教育聯盟 (HOTTEA)
Health Outcomes and Technology Teaching and Education Alliance
報名網址